安全性情報(臨床開発・製販後GVP)関連の転職・求人情報
JAC Recruitmentが採用企業からお預かりしている求人の中からWEBに掲載可能な安全性情報(臨床開発・製販後GVP)関連求人特集です。また、ハイクラス求人に関してはWEBには掲載できない非公開求人も多数保有しております。これまで培った経験やスキルを活かした転職をお考えの際はぜひ当社の転職サポートをご利用ください。
Life Sciences BPO (Business Process Outsourcing) Services Team Lead/外資系製薬企業向けファーマコビジランス業務(安全性定期報告)チームリード(LS2514)
- 採用企業名
- 非公開
- 職種
-
メディカル・バイオ - 臨床開発QC・GCP監査
メディカル・バイオ - 薬事申請
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
【職務について】
グローバル製薬業界で高い評価を得ている弊社のLife Sciences Unitは、今後の成長・拡大が期待されている事業部門です。外資系を含む日本の製薬企業を顧客ターゲットとし、IT
...
- 求める経験
-
【Must】
・安全性定期報告書作成、措置報告、研究報告のPV業務経験 3年以上
*文献スクリーニング経験のみでも応募可
・医薬品業界またはCROでの勤務経験
・規制(例:GCP、ICH、GVP、GP
...
- 年収
-
600万円 - 1200万円
- 語学力
-
英語力:中級以上
語学:日本語
ネイティブレベルの日本語力
ビジネスレベルの英語力(ライティング、スピーキング、リーディング)
詳細へ
■Manager, Pharmacovigilance
- 採用企業名
- 非公開
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府 東京都
- 仕事内容
-
■医薬品安全性監視部門(PVG)におけるProject ManagementおよびLine Management業務全般
《主な業務》
・安全性情報管理(医薬品の臨床試験・市販後)のプロジェクトマネ
...
- 求める経験
-
・ビジネスレベル以上の日本語・英語能力(読み書きと会話)
⇒顧客やグローバルチームと英語で会議ができるレベル
・CROまたは製薬メーカーにおける、Project ManagementまたはLine
...
- 年収
-
800万円 - 1500万円
- 語学力
-
読み書きは実務上発生する。
会話については即時求めないものの、今後PPDグローバル全体で部署会議が発生する可能性もあり、まずはヒアリングに抵抗がないことを求めます。(急にコミュニケーションを求めることはしません。レベルに合わせた業務範囲を求めます)
詳細へ
安全性担当者 【東証グロース市場 上場済みバイオベンチャー】
- 採用企業名
- 非公開
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
メディカル・バイオ - 製造販売後調査(GPMSP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
<職務>
・開発中のパイプラインの上市に向けて、安全性業務全般を担当いただきます。
<おもな業務内容>
・GVP 業務の管理と手順書に従った執行(製造販売後安全管理業務手順書(GVP)、細則、様式集
...
- 求める経験
-
【必須】
・安全性情報の業務経験5年以上
・英語力(読み書き可能なレベル)
・医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律”、GVP 省令、等、医薬品製造販売に関する各種法令、ガイド
...
- 年収
-
600万円 - 1200万円
- 語学力
-
英語力:初級以上
詳細へ
安全管理責任者候補 【東証グロース市場 上場済みバイオベンチャー】
- 採用企業名
- 非公開
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
メディカル・バイオ - 製造販売後調査(GPMSP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
<職務>
・開発中のパイプラインの上市に向けて、安全性業務全般を担当いただきます。
・入社後は、医薬品製造販売業三役の一角として、法令に基づく安全性に関する業務の統括、執行を行う責任者をお任せする可
...
- 求める経験
-
【必須】
・安全性情報の業務経験10年以上
・英語力(読み書き可能なレベル)
・医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律”、GVP 省令、等、医薬品製造販売に関する各種法令、ガイ
...
- 年収
-
800万円 - 1500万円
- 語学力
-
英語力:初級以上
詳細へ
クオリティーマネジメントスペシャリスト
- 採用企業名
- ロシュ・ダイアグノスティックス株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
メディカル・バイオ - メディカルGQP・GMP・品質保証・品質管理
メディカル・バイオ - 品質保証
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
【職務内容】
弊社製品(免疫・生化学・遺伝子・病理検査関連の試薬、医療機器など)の市販後安全管理
・品質保証メンバーとして以下の業務を行います。
● GVP省令に基づく体外診断用医薬品、医療機器の
...
- 求める経験
-
【求める経験】
以下のいずれかの経験を有すること
● 体外診断用医薬品・医療機器・医薬品等における品質保証・安全管理業務、または品質管理関連の経験(3年以上)
● 体外診断用医薬品・医療機器・医薬品等
...
- 年収
-
600万円 - 1200万円
- 語学力
-
英語力:初級以上
詳細へ
ファーマコビジランス職(グローバルPV渉外管理担当)
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
●グローバルPVの渉外管理担当
・グローバルPV契約の締結・維持・管理
・グローバルPV-SOPの維持・管理
●海外子会社・海外提携会社と連携し、グローバルPV systemの維持・管理・改善の推
...
- 求める経験
-
<必須>
●安全管理統括部門でPV契約管理、PV-SOP管理、PV-regulatory intelligence、PVトレーニング等の業務、症例評価・対策業務から一つもしくは複数を経験したことがある
...
- 年収
-
600万円 - 1100万円
- 語学力
-
英語力:上級以上
TOEIC:800点以上
詳細へ
ファーマコビジランス職(グローバルPV企画担当)
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
●グローバルPV企画・管理業務
●海外子会社(特にアジア地域)のPV業務の管理・オーバーサイト
・海外子会社PV担当者と連携し、グローバル基準に準拠したローカルでのPV systemの維持・管理
●
...
- 求める経験
-
<必須>
●安全評価・対策業務、PV契約管理、PV査察・オーディット対応などから一つもしくは複数を経験したことがある即戦力
●GVP、ICH等関連法規・規制等をグローバルレベルで経験されたことがある方
...
- 年収
-
600万円 - 1100万円
- 語学力
-
英語力:上級以上
TOEIC:860点以上
詳細へ
薬剤疫学担当者
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
以下に関して、グローバルを含めて取り組む
・RWDを活用した、クリニカルクエスチョンに対する情報創出
・RWDを活用した、安全対策の効果確認(医療従事者等の意識調査を含む)
・シグナルディテクション/
...
- 求める経験
-
<必須>
・薬剤疫学(統計知識を含む)の専門性
・SAS、R、Pythonを用いたデータセット構築及び解析の経験
<望ましい>
・オンコロジー領域の経験
・プロジェクトマネジメントの経験
<必須>
...
- 年収
-
700万円 - 1100万円
- 語学力
-
英語力:中級以上
TOEIC:700点以上
詳細へ
ファーマコビジランス職(グローバルPV企画担当)
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
グローバルPV企画・管理業務
海外子会社(特にアジア地域)のPV業務の管理・オーバーサイト
海外子会社PV担当者と連携し、グローバル基準に準拠したローカルでのPV systemの維持・管理
海
...
- 求める経験
-
<必須>
安全評価・対策業務、PV契約管理、PV査察・オーディット対応などから一つもしくは複数を経験したことがある即戦力
GVP、ICH等関連法規・規制等をグローバルレベルで経験されたことがある方
...
- 年収
-
700万円 - 1100万円
- 語学力
-
英語力:上級以上
TOEIC:860点以上
詳細へ
安全対策・メディカルドクター職
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
医療・介護・福祉 - 医師
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
抗がん剤の開発プロジェクトへの参画もしくは上市後間もない抗がん剤を担当し、以下の安全対策業務に従事する。
① 副作用・有害事象症例の安全性評価と臨床試験における安全対策の検討
② RMP(医薬品リスク
...
- 求める経験
-
<必須>
・企業文化を理解し、企業の組織人として従事することに抵抗がない
(真摯さ、誠実さ,チームプレーの経験,適切なリーダーシップ)
・ 英語での不自由のないコミュニケーション
<望ましい>
・がん
...
- 年収
-
1200万円 - 1600万円
- 語学力
-
英語力:中級以上
TOEIC:700点以上
詳細へ
ファーマコビジランス職(安全対策)
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
業務経験、本人の希望等を総合的に判断の上、下記の中から業務をアサイン。
治験の安全性モニタリング(安全性管理)業務
申請資料(安全性パート:RMP案、添付文書案)作成・レビュー
市販後安全
...
- 求める経験
-
<必須>
安全対策業務経験者(3年以上)
医学・薬学に関する基本的知識とPV関連規制等の理解・習熟
当局・他社・他部所との折衝が出来る交渉力
日常業務において、コンプライアンスを遵守し
...
- 年収
-
700万円 - 1100万円
- 語学力
-
英語力:中級以上
TOEIC:650点以上
詳細へ
ファーマコビジランス職(症例評価/症例プロセス)
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
業務経験、本人の希望等を総合的に判断の上、下記の中から業務をアサイン。
症例評価関連プロジェクトやチームのマネジメント/リード
安全管理情報のデータ収集および症例評価プロセスの管理・運用、安全
...
- 求める経験
-
<必須>
リーダーシップ、プロジェクトマネジメント能力・経験(プロジェクトやチームのマネジメント/リードの経験)
安全性評価業務経験者(3年以上)
英語:グローバル会議等ビジネスで使用して
...
- 年収
-
700万円 - 1100万円
- 語学力
-
英語力:中級以上
TOEIC:750点以上
詳細へ
GCP監査
- 採用企業名
- 第一三共株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
◆GCP(臨床試験)領域における監査担当者として、医療機関監査、総括報告書監査、TMF監査、ベンダー監査、システム監査、などのGCP監査を計画・実施し、監査報告書を作成し、監査所見に対するCAPA(是
...
- 求める経験
-
・製薬企業又はCROにおいて、5年以上のGCP(臨床試験)領域の監査業務の実務経験がある
・GCP関連規制に関する知識(ICHや国内外規制)を有し、臨床試験プロセス全般に精通している
・柔軟な思考とチ
...
- 年収
-
700万円 - 1100万円
- 語学力
-
英語力:中級以上
TOEIC:700点以上
詳細へ
安全性情報プロジェクトマネージャー【関西窓口】
- 採用企業名
- IQVIAサービシーズ ジャパン合同会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
メディカル・バイオ - メディカルサイエンスリエゾン
メディカル・バイオ - メディカルアフェアーズ
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府 東京都
- 仕事内容
-
■医薬品等安全性情報管理(臨床試験・市販後)のプロジェクトマネジメントと、そのサービスレベルの担保・維持を担います。 顧客窓口として、実働チームのオーバーサイトを通じ、顧客に対してシームレスで可視性の
...
- 求める経験
-
•ライフサイエンス、または、関連分野における大卒以上の学歴
■下記いずれかのご経験必須
•CROまたは製薬メーカーにおける、4年以上の安全性情報管理(ファーマコビジランス、メディカルインフォメーショ
...
- 年収
-
800万円 - 1450万円
- 語学力
-
英語力:中級以上
詳細へ
Pharmacovigilance Project Manager/ Lifecycle & Safety/ IQVIA Services
- 採用企業名
- 非公開
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
東京都
- 仕事内容
-
■Purpose
医薬品等安全性情報管理(臨床試験・市販後)のプロジェクトマネジメントと、そのサービスレベルの担保・維持を担います。 顧客窓口として、実働チームのオーバーサイトを通じ、顧客に対してシー
...
- 求める経験
-
■Required Knowledge, Skills and Abilities
ビジネスレベル以上の日本語・英語能力(読み書き、会話とも)
チーム管理とリーダーシップスキル、問題解決スキル。
プロ
...
- 年収
-
800万円 - 1320万円
- 語学力
-
英語力:中級以上
TOEIC:700点以上
詳細へ
【安全性情報】Line Manager
- 採用企業名
- IQVIAサービシーズ ジャパン株式会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府 東京都
- 仕事内容
-
■安全性情報部門にてラインマネジメントをご担当頂きます。
* 要員計画、業務配分、業務の指導などを通じて、担当するチーム(10~20名程度)のラインマネジメントを行う。
* メンバーとの定期的なコミュ
...
- 求める経験
-
■必須
* 医薬品・医療機器の安全性情報管理に関する、症例マネジメント経験
* ケースプロセッシング業務における品質・生産性改善の経験
* マネージャー、リーダー、メンター、教育担当など、何らかの人的
...
- 年収
-
800万円 - 1450万円
- 語学力
-
英語力:中級以上
詳細へ
安全性情報 オペレーション(スタッフ~リード)
- 採用企業名
- IQVIAサービシーズ ジャパン合同会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府 東京都
- 仕事内容
-
■ 治験または市販後/追加調査に関する、医薬品または医療機器の安全性情報管理プロジェクトのメンバーとして以下のCase processingタスクを担当いただきます。
- 有害事象に関する情報の受領、
...
- 求める経験
-
■必須
<Operations Specialist>
・安全性情報ケースプロセッシング(入力、トリアージ、評価、QC)経験が1年以上有ること(入力のみでも応募可)
・ビジネスレベルの日本語能力
・
...
- 年収
-
400万円 - 1000万円
- 語学力
-
英語力:中級以上
詳細へ
Pharmacovigilance Specialist/ IQVIA Services
- 採用企業名
- 非公開
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府 東京都
- 仕事内容
-
■担当業務(担当者相当のポジション)
* 医薬品/医療機器の治験/市販後に関する、以下の安全性情報管理業務。
- 安全性情報の受領・トリアージ・発番・データベース入力・PMDA報告要否の一次評価・QC
...
- 求める経験
-
■必須
* 安全性情報ケースプロセッシング(受領、トリアージ、発番、内容確認、データベースへの入力/QC)経験が1年以上有ること
(受領、発番など、限定的なご経験のみでも歓迎します)
* ビジネスレ
...
- 年収
-
420万円 - 1000万円
- 語学力
-
英語力:中級以上
詳細へ
安全性情報 / Line Manager
- 採用企業名
- IQVIAサービシーズ ジャパン合同会社
- 職種
-
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府 東京都
- 仕事内容
-
■安全性部門のラインマネージャーとして業務担当者の管理、サポートを行います。
具体的には、
安全性メンバーのパフォーマンス管理、リソース管理、顧客納品のタイムライン管理、品質管理も含まれます。
また
...
- 求める経験
-
・ヘルスサイエンス関連の大学卒および6年以上の安全性関連業務の実務経験者。
・安全性業務(症例評価、様式作成)の実務、システムに関する経験と知識
・安全性関連の規制に関する深い知識 例)日本の規制要件
...
- 年収
-
800万円 - 1450万円
- 語学力
-
英語力:中級以上
詳細へ
臨床開発および安全管理に係るグローバル品質保証業務のリード
- 採用企業名
- 日系製薬メーカー
- 職種
-
メディカル・バイオ - 臨床開発QC・GCP監査
メディカル・バイオ - 安全性情報(臨床開発・製販後GVP)
メディカル・バイオ - 品質保証
- 雇用形態
- 無期雇用
- 勤務地
-
大阪府
- 仕事内容
-
グローバル品目のGCP/PV QA担当業務に加え,自社におけるグローバル臨床開発及び安全管理に係る品質保証業務レベル向上のため、必要なガバナンス体制の構築と運営、および課題抽出とその解決のための解決策
...
- 求める経験
-
【必須要件】
- 英語(ビジネスレベル)
- GCP/PVに関連するレギュレーション・品質マネジメントシステムの理解
- GCP臨床施設監査・受審スキル
【望ましい要件】
- ライフサイエンス業界で
...
- 年収
-
1280万円 - 非公開
- 語学力
-
英語力:中級以上
詳細へ
WEBではお伝えできない情報を、
戦略的な観点からお伝えします
JACでは、気になる企業の
同業他社との比較により、その企業や求人の採用傾向など
特長をより明確に知ることができます。
| 求人の観点 |
A社 |
B社 |
CD社・・ |
| 採用される方の属性 |
XXXX |
XXXX |
|
| 採用される/されない方の違い |
XXXX |
XXXX |
|
| 実年収の高低 |
XXXX |
XXXX |
|
| 企業の戦略・成長性 |
XXXX |
XXXX |
|
JACでは、約1,000名ものコンサルタントが直接企業とコンタクトをとり、
求人のスペックだけではなく、社風や部・課・チームの雰囲気など気になる情報もお伝えしております。
| 求人の観点 |
A社 |
B社 |
CD社・・ |
| 年収傾向 |
XXXX |
XXXX |
|
| 社内・部内の雰囲気 |
XXXX |
XXXX |
|
| 上司の傾向 |
XXXX |
XXXX |
|
| 本社・支社の関係性 |
XXXX |
XXXX |
|
JACは複数のコンサルタントが
あなたをスカウト
複数のコンサルタントがサポートするJACのコンサルティング
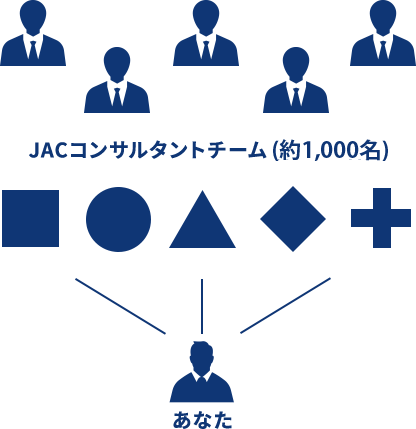
各職種のプロが多角的に
求人を紹介するので、
幅広い選択肢からお選び頂けます。
特定のコンサルタントが担当する一般的な外資系エージェント
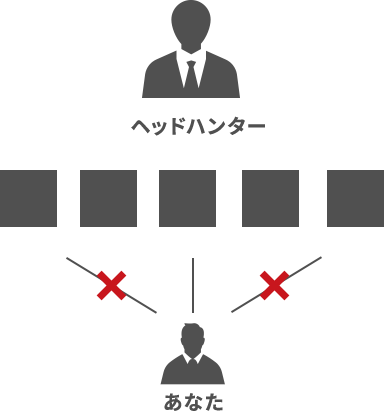
一人のヘッドハンターが選んだ
求人だけなので
偏りや漏れが出ることがあります。






